
深度整合研发经验,不断攀登研发技术高峰,搭建新药研发一体化创新服务平台。
抗体-寡核苷酸偶联物 (AOC) 代表了一种变革性的治疗模式,它将抗体的精准靶向能力与寡核苷酸(如siRNA、ASO)的基因沉默或调控功能相结合。通过抗体部分特异性识别疾病相关组织或细胞表面的抗原,AOC能够实现对寡核苷酸的定向递送,从而克服传统寡核苷酸药物在细胞内吞效率低、组织穿透性差以及脱靶效应等关键瓶颈。
 美迪西AOC服务平台优势
美迪西AOC服务平台优势

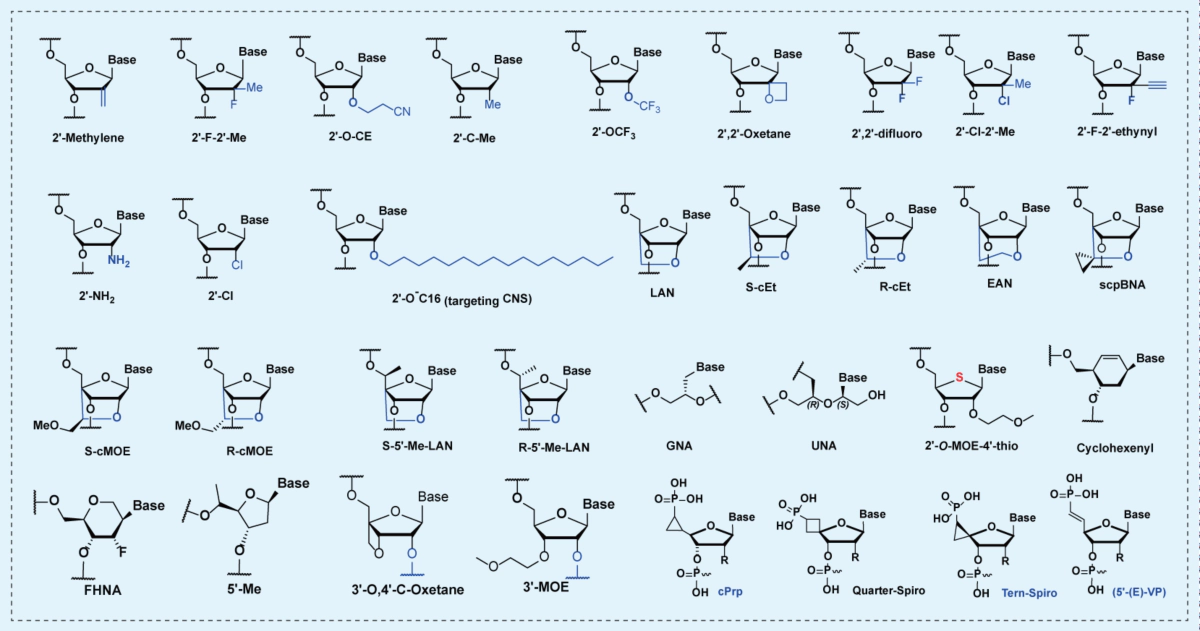
 专业偶联&案例验证
专业偶联&案例验证



 案例分享:合成与表征
案例分享:合成与表征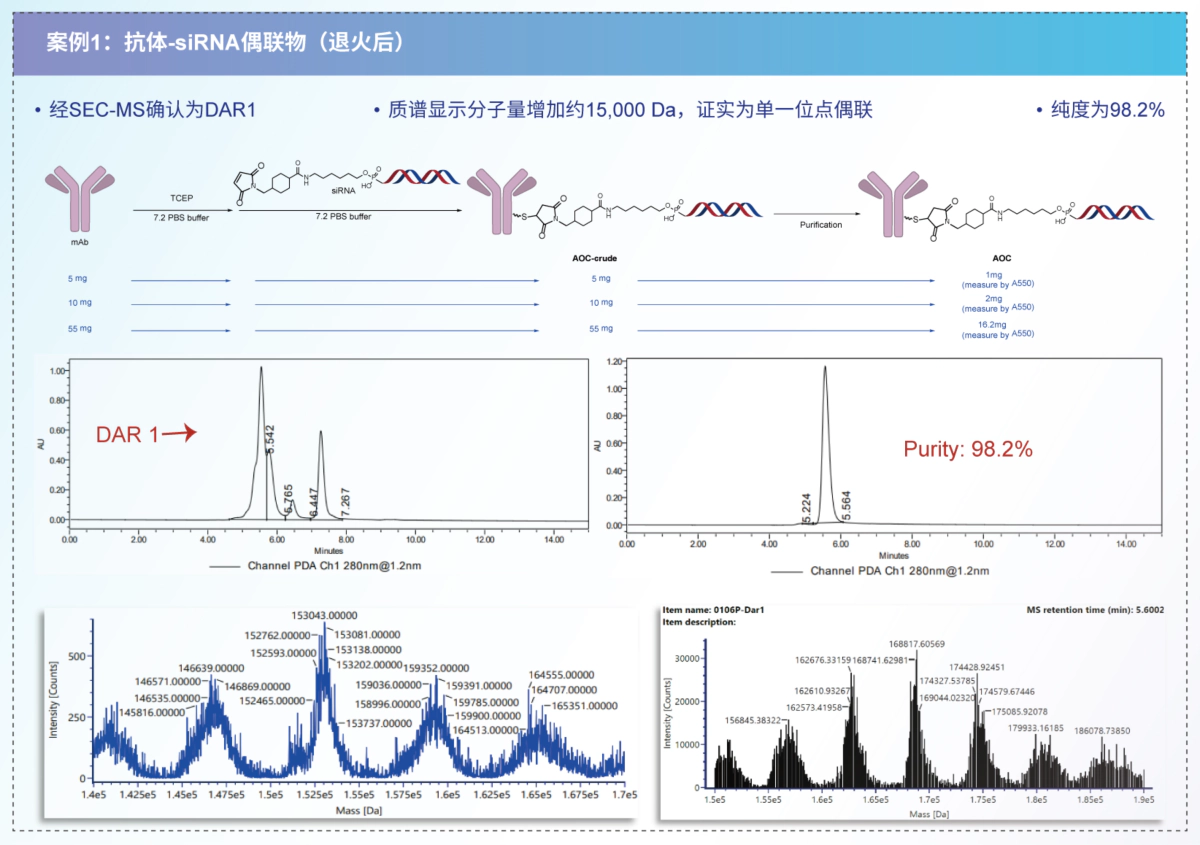

 从药物发现到IND申报⸺提供一站式临床前服务
从药物发现到IND申报⸺提供一站式临床前服务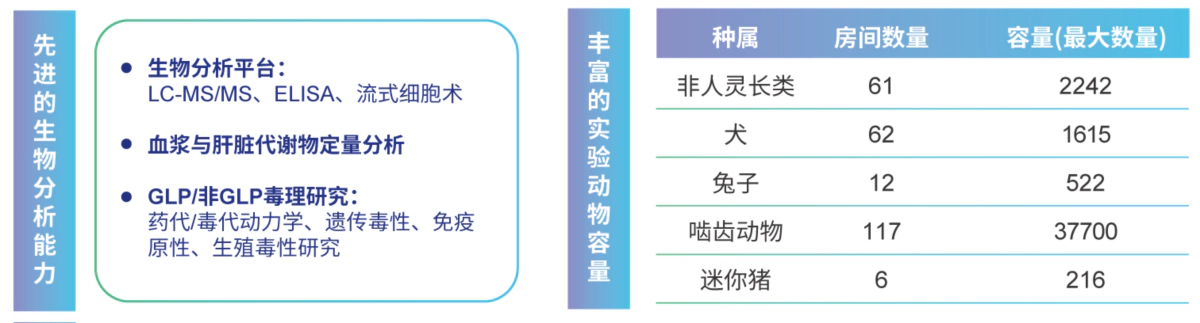
 FAQs
FAQs小核酸药物虽然在靶向肝脏细胞/组织中已取得重大进展,但无法解决肝脏以外的药物靶向递送问题。同时,在给药剂量、体内暴露浓度与时间窗等方面仍需要进一步优化。
抗体对肿瘤细胞抗原具有高特异性和高亲和力,使其成为药物靶向递送的理想载体,可以将药物精准靶向递送至肿瘤病灶部位。
AOC技术不仅是解决递送难题的关键,更有望催生突破性疗法,为目前无药可治的疾病带来新的希望。
抗体寡核苷酸偶联物(AOC)与 RNAi 药物开发面临序列设计低效、偶联策略单一、规模化合成困难、精准表征缺失、体内评价不完善等关键问题,具体包括:
序列设计:难以精准定位 mRNA 最优沉默窗口,特异性与跨物种同源性难以兼顾,siRNA/ASO 设计效率低。
合成与偶联:寡核苷酸规模化合成能力不足,缺乏多样化、位点特异性的抗体 - 寡核苷酸偶联技术,难以稳定控制 DAR 值(药物抗体比)。
交付体系:缺乏 GalNAc(N-乙酰半乳糖胺)、可电离脂质等高效递送载体开发能力,难以实现寡核苷酸药物高效递送。
美迪西团队已建立 RNAi-AOC 研发服务平台,面向肝外靶向递送需求,覆盖从序列设计、寡核苷酸制备、抗体-寡核苷酸偶联,到纯化表征与体内外评价的全流程开发。核心能力如下:
AI序列设计(MOD):预测最优沉默窗口,综合结构可及性、特异性与跨物种同源性分析,高效输出适用于 AOC 开发的 siRNA/ASO 候选序列。
规模化寡核苷酸合成与载荷制备:具备从 OD 到 mg、g 级别的寡核苷酸合成与纯化能力,可为 AOC 开发提供高质量 oligonucleotide payload,并支持不同阶段的工艺放大与样品供应。
多类型 AOC 偶联工艺开发:建立了涵盖点击化学(DBCO-叠氮)、马来酰亚胺-巯基偶联、氨基-寡核苷酸-抗体偶联(AOAC)及基于微生物谷氨酰胺转胺酶(mTGase)或抗体位点突变的定点偶联等多样化偶联体系,可根据抗体、linker 与 oligonucleotide 的结构特征灵活选择工艺路径,支持面向肝外靶向的 AOC 分子构建。
AOC 纯化与高分辨表征分析:配备 AEX、SEC、UPLC-MS、TOF 等分析纯化平台,可用于偶联产品纯化、DAR 分布分析、分子量确认及杂质表征,支持 AOC 产品质量研究与工艺优化。
从分子构建到体内外评价的闭环开发:整合化学修饰、偶联工程、分析表征及体内 DMPK/药效评价能力,形成面向肝外递送 AOC 分子的端到端研发支持体系,加快候选分子的发现、筛选与转化。
<i id='b8400'><strike id='d755b'><tt id='8576f'><pre id='345c6'></pre></tt></strike></i>